La insuficiencia cardíaca con fracción de eyección reducida (HFrEF) es un tipo importante de insuficiencia cardíaca, y el estudio China HF demostró que el 42% de las insuficiencias cardíacas en China son HFrEF, aunque hay varias clases terapéuticas estándar de medicamentos disponibles para la HFrEF que han reducido el riesgo. de muerte y hospitalización por insuficiencia cardíaca en cierta medida. Sin embargo, los pacientes tienen un alto riesgo de sufrir episodios recurrentes de empeoramiento de la insuficiencia cardíaca, la mortalidad se mantiene en torno al 25% y el pronóstico sigue siendo malo. Por lo tanto, todavía existe una necesidad urgente de nuevos agentes terapéuticos en el tratamiento de la HFrEF, y en el estudio VICTORIA se estudió Vericiguat, un nuevo estimulador de guanilato ciclasa soluble (sGC), para evaluar si Vericiguat podría mejorar el pronóstico de los pacientes con HFrEF. El estudio es un estudio de resultados clínicos de fase III multicéntrico, aleatorizado, de grupos paralelos, controlado con placebo, doble ciego y basado en eventos. Realizado bajo los auspicios del Centro VIGOR en Canadá en colaboración con el Instituto de Investigación Clínica de Duke, participaron en el estudio 616 centros en 42 países y regiones, incluidos Europa, Japón, China y Estados Unidos. Nuestro departamento de cardiología tuvo el honor de participar. Un total de 5.050 pacientes con insuficiencia cardíaca crónica de ≥18 años, clase II-IV de la NYHA, FE <45%, con niveles elevados de péptido natriurético (NT-proBNP) dentro de los 30 días previos a la aleatorización y que habían sido hospitalizados por insuficiencia cardíaca. dentro de los 6 meses anteriores a la aleatorización o se les administraron diuréticos por vía intravenosa para la insuficiencia cardíaca dentro de los 3 meses anteriores a la aleatorización se inscribieron en el estudio, todos recibieron ESC, AHA/ACC y nacional/región pautas específicas recomiendan el estándar de atención. Los pacientes fueron asignados al azar en una proporción de 1:1 a dos grupos y se les administróVericiguat(n=2526) y placebo (n=2524) además de la terapia estándar, respectivamente.
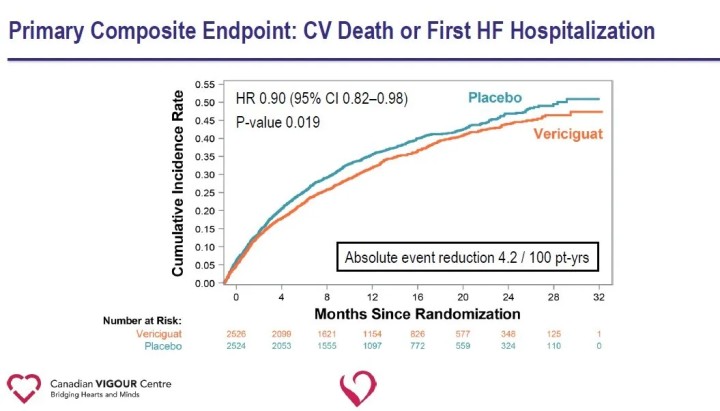
El criterio de valoración principal del estudio fue el criterio de valoración compuesto de muerte cardiovascular o primera hospitalización por insuficiencia cardíaca; los criterios de valoración secundarios incluyeron componentes del criterio de valoración principal, la primera y posteriores hospitalizaciones por insuficiencia cardíaca (primeros eventos y recurrentes), el criterio de valoración compuesto de muerte por todas las causas u hospitalización por insuficiencia cardíaca y muerte por todas las causas. En una mediana de seguimiento de 10,8 meses, hubo una reducción relativa del 10% en el criterio de valoración principal de muerte cardiovascular o primera hospitalización por insuficiencia cardíaca en el grupo de Vericiguat en comparación con el grupo de placebo.
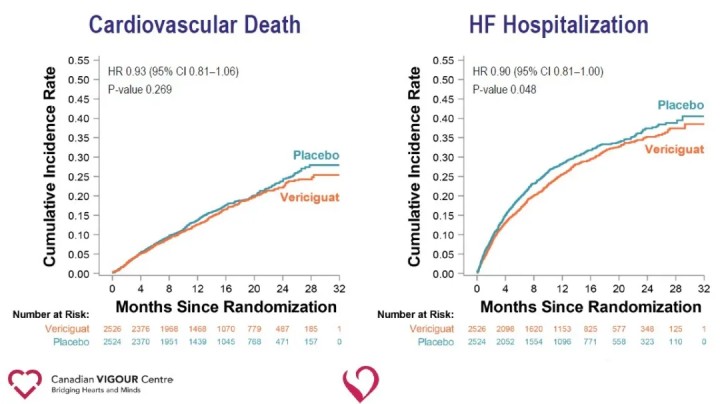
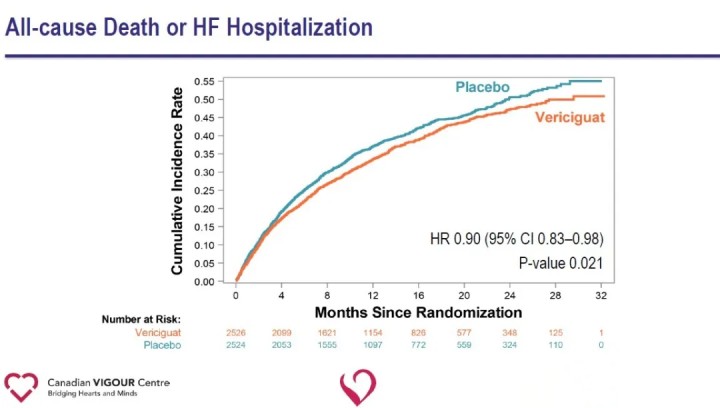
El análisis de los criterios de valoración secundarios mostró una reducción significativa en las hospitalizaciones por insuficiencia cardíaca (HR 0,90) y una reducción significativa en el criterio de valoración compuesto de muerte por todas las causas u hospitalización por insuficiencia cardíaca (HR 0,90) en el grupo de Vericiguat en comparación con el grupo de placebo.
Los resultados del estudio sugieren que la adición deVericiguatEl tratamiento estándar de la insuficiencia cardíaca reduce significativamente la aparición reciente de episodios de insuficiencia cardíaca que empeoran y reduce el riesgo del criterio de valoración compuesto de muerte cardiovascular u hospitalización por insuficiencia cardíaca en pacientes con HFrEF. La capacidad de Vericiguat para reducir el riesgo del criterio de valoración compuesto de muerte cardiovascular u hospitalización por insuficiencia cardíaca en pacientes con insuficiencia cardíaca de alto riesgo proporciona una nueva vía terapéutica para la insuficiencia cardíaca y abre nuevas vías para la exploración futura de la enfermedad cardiovascular. Actualmente, vericiguat no está aprobado para su comercialización. La seguridad, eficacia y rentabilidad del fármaco aún deben probarse más en el mercado.
Hora de publicación: 09-feb-2022
